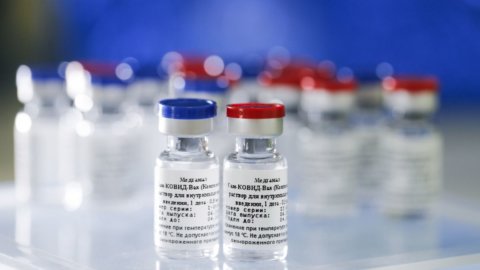
何週間にもわたる疑わしいためらいの後、必要性が不信に勝った。 ワクチンは必要であり、すぐに必要です。 L'エマ したがって、ロシアのワクチンのローリングレビュープロセス(イタリア語で継続的なレビュー)を開始することを決定しました スプートニク V. 発表は本日、欧州医薬品庁自体から メモ その中で彼は、「EMA は一般的なタイミングを予測することはできませんが、段階的な審査中に行われた作業により、申請の可能性を評価するのに通常よりも時間がかからないはずです」と明言しています。
ロシア当局は、EMA からの連絡の直後に、 50万回分を供給する準備ができています XNUMX月に始まるヨーロッパ人へのワクチンの。
ローリングレビューは、規制当局が 通常の評価プロセスをスピードアップする 薬とワクチンの。 簡単に言えば、通常の状況では、企業が医薬品やワクチンの販売許可を申請する際に製品に関するすべてのデータ (有効性、安全性、品質など) を提示する場合、継続的なレビューにより、これらのデータは早期に、すでに実験中に検討されます。段階。 データが利用可能になった時点でデータを分析することで、EMA は時間を稼ぎ、ワクチンを使用できるかどうかをより迅速に決定する機会を得ることができます。 現在配布されているワクチン (モデルナ、ファイザー、アストラゼネカ) も継続的な審査を受けており、現在、ドイツの製薬会社 Novavax の血清も審査を受けています。 到着はXNUMX月の予定です.
スプートニクに戻ると、「EMA は、機関のメモを読み、データが利用可能になり次第評価します。 メリットがリスクを上回るかどうかを判断します。 ローリングレビューは、正式な販売承認申請に十分な証拠が得られるまで続けられます。」
ワクチンは、「通常の EU 基準」に基づいてテストされます。 有効性、安全性、品質代理店は、「ワクチンの製造販売承認申請書が提出されました」と通知します。
ロシアの血清は、ロシアの国立疫学および微生物学センターであるガマレヤによって開発されましたが、改訂の要求は、ロシアの製薬グループのドイツ支部であるR-Pharmから来ました. それは ウイルスベクターワクチン XNUMX回の投与で投与されます(それぞれ異なるウイルスベクターを使用)。 モスカによると、血清は Covidに対する有効性は90%に等しい. 同じデータが、世界で最も権威のある科学雑誌の XNUMX つである The Lancet に掲載されました。
現在、ワクチンはロシアだけでなく、アルゼンチン、ボリビア、ベネズエラ、ハンガリー、セルビア、アルジェリア、パレスチナ、ベラルーシでもすでに使用されています。
一方、ワクチンに関するニュースはイタリアからも届いています。 イタリアは、アストラゼネカのワクチン投与量の輸出を拒否した最初の EU 加盟国です。 ブリュッセルで学んだことによると、金曜日にイタリア当局は欧州委員会に、製薬会社からオーストラリアへのワクチンの出荷をブロックする決定を通知しました。
一方、回覧を通じて、保健省の予防総局は、ワクチンを受ける少なくともXNUMX〜XNUMXか月前にCovidに感染した人は、 XNUMX回ではなく、XNUMX回だけ投与されました。
「上級保健評議会のSARS-Cov-2感染に関する常設グループによって表明された意見を考えると」、「23年02月2021日にアイファによって表明された意見に従って、検討することが可能であることが示されています。 SarsCoV-2/Covid-19ワクチンの単回投与 以前にSARS-CoV-2に感染した被験者 (有症状または無症候性で)ワクチン接種が記録された感染の少なくとも3か月後、できれば6か月以内に行われることを条件とします。」
ただし、この新規性は、薬物療法による一次的または二次的な免疫不全状態の被験者には適用されません。